Gängige Reaktionstypen von homogenen Edelmetallkatalysatoren
Einführung
Edelmetalle wie Platin, Palladium, Rhodium und Gold werden aufgrund ihrer hohen katalytischen Aktivität, Selektivität und Stabilität häufig als homogene Katalysatoren verwendet. Sie sind auch für ihre hohe thermische Stabilität und chemische Inertheit bekannt, was sie zu außergewöhnlichen Katalysatoren macht. Aufgrund dieser Eigenschaften finden homogene Edelmetallkatalysatoren ein breites Spektrum an Anwendungen, z. B. in der Pharmazie, Petrochemie, Chemie und den Materialwissenschaften.
In diesem Artikel werden wir über die üblichen Reaktionstypen von homogenen Edelmetallkatalysatoren sprechen. Wir hoffen, dass Sie ein besseres Verständnis für diese wertvollen Katalysatoren bekommen.

Abbildung 1. Edelmetallkatalysatoren
Häufige Reaktionstypen von homogenen Edelmetallkatalysatoren
Homogene Edelmetallkatalysatoren werden für eine Vielzahl von Reaktionen eingesetzt. Typische Beispiele sind Hydrierungen, Hydroformylierungsreaktionen, Kupplungsreaktionen usw.
-Hydrierung:
Die Hydrierung ist eine Reaktion, bei der ungesättigten organischen Verbindungen Wasserstoff zugesetzt wird, in der Regel mit Hilfe eines Katalysators. Homogene Katalysatoren wie Platin und Palladium werden in Hydrierungsreaktionen häufig verwendet, um Alkene in Alkane und Nitroverbindungen in Amine umzuwandeln.

Abbildung 2. Metallkatalysierte Hydrierungs- und Dehydrierungsreaktionen für eine effiziente Wasserstoffspeicherung [1]
--Dehydrierung:
Die Dehydrierung ist das Gegenteil der Hydrierung, bei der Wasserstoff aus einem Molekül entfernt wird. Edelmetallkatalysatoren wie Platin und Rhodium werden in Dehydrierungsreaktionen eingesetzt, um Alkene aus Alkanen und Carbonylverbindungen aus Alkoholen zu erzeugen.
-Oxidation:
Bei Oxidationsreaktionen verliert ein Molekül Elektronen, und homogene Edelmetallkatalysatoren werden verwendet, um Alkohole in Aldehyde oder Ketone und Alkene in Epoxide umzuwandeln. Unter diesen Oxidationsreaktionen ist das "Hoechst-Wacker"-Verfahren das bekannteste, bei dem Acetaldehyd aus Ethen und Sauerstoff mit Hilfe von Pd/Cu-Katalysatoren in wässrigen, chloridhaltigen Lösungen synthetisiert wird.
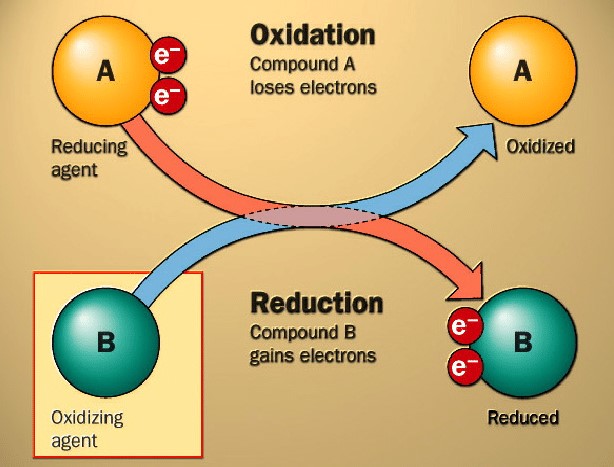
Abbildung 3. Grundlegende Oxidation und Reduktion [2]
-Reduktion:
Die Reduktion ist das Gegenteil der Oxidation, bei der ein Molekül Elektronen gewinnt. Diese homogenen Katalysatoren werden im Allgemeinen bei Reduktionsreaktionen eingesetzt, um Nitroverbindungen in Amine und Carbonylverbindungen in Alkohole umzuwandeln.
--Kupplung:
Bei Kupplungsreaktionen werden zwei oder mehr Moleküle zu einem größeren Molekül verbunden. Palladium, Platin und andere Katalysatoren werden bei Kupplungsreaktionen eingesetzt, um Kohlenstoff-Kohlenstoff-Bindungen zu bilden, wie z. B. bei der Suzuki-Reaktion und der Heck-Reaktion.
--Carbonylierung:
DieCarbonylierung bezieht sich auf Reaktionen zur Bildung von Aldehyden, Ketonen usw. unter Verwendung von Kohlenmonoxid (CO). Das bekannteste Verfahren ist die Carbonylierung von Methanol zu Essigsäure. Er wird auch Monsanto-Prozess genannt . Alle diese Prozesse können ohne Rhodiumkatalysatoren nicht durchgeführt werden.
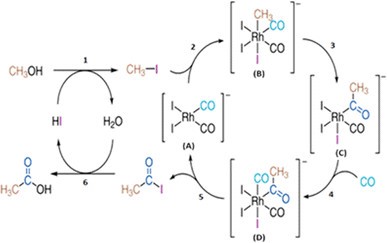
Abbildung 4. Vorgeschlagene katalytische Zyklen der rhodiumkatalysierten Methanolcarbonylierungsreaktion (Monsanto-Prozess) [3]
-Hydroformylierung:
DieHydroformylierung ist auch als Oxosynthese bekannt. Bei diesem Verfahren werden Alkene mit einer Mischung aus Kohlenmonoxid (CO) und Wasserstoff (H2) in Aldehyde umgewandelt. Rhodiumkatalysatoren haben bei diesen Verfahren den früheren Kobaltkatalysator abgelöst.
-Isomerisierung:
Die Isomerisierung ist eine Reaktion, bei der ein Molekül eine strukturelle Umordnung erfährt. Platin und Rhodium sind typische homogene Katalysatoren, die in Isomerisierungsreaktionen zur Umwandlung von Alkanen in verzweigte Alkane und von Alkenen in Isomere verwendet werden.
In der nachstehenden Tabelle finden Sie weitere Informationen über den Vergleich zwischen den verschiedenen Reaktionstypen homogener Edelmetallkatalysatoren.
Tabelle 1. Verschiedene Reaktionstypen von homogenen Edelmetallkatalysatoren
|
|
Definition |
Beispiele |
|
Hydrierung |
Hinzufügen von Wasserstoff; |
Umwandlung von Alkenen zu Alkanen und von Nitroverbindungen zu Aminen; |
|
Dehydrierung |
Entfernen von Wasserstoff; |
Umwandlung von Alkanen in Alkene und von Alkoholen in Carbonylverbindungen; |
|
Oxidation |
Verlust von Wahlen; |
Umwandlung von Alkoholen in Aldehyde oder Ketone und von Alkenen in Epoxide; |
|
Reduktion |
Gewinnung von Elektronen; |
Umwandlung von Nitroverbindungen in Amine und von Carbonylverbindungen in Alkohole; |
|
Kopplung |
Verknüpfung von zwei oder mehr Molekülen zu einem größeren Molekül; |
Die Suzuki-Reaktion und die Heck-Reaktion; |
|
Carbonylierung |
Bildung von Aldehyden und Ketonen mit Hilfe von Kohlenmonoxid (CO); |
Das Monsanto-Verfahren; |
|
Hydroformylierung |
Umwandlung von Alkenen in Aldehyde mit Kohlenmonoxid (CO) und Wasserstoff (H2); |
Verwendung von Rhodium-Katalysatoren; |
|
Isomerisierung |
Strukturelle Anordnungen; |
Umwandlung von Alkanen in verzweigte Alkane und von Alkenen in Isomere; |
Schlussfolgerung
Kurz gesagt, homogene Edelmetallkatalysatoren werden in vielen chemischen Reaktionen eingesetzt, einschließlich Hydrierung, Dehydrierung, Oxidation, Reduktion, Kupplung, Carbonylierung, Hydroformylierung und Isomerisierung. Ihre hohe katalytische Aktivität, Selektivität und Stabilität machen sie zu unschätzbaren Werkzeugen für Chemiker in der pharmazeutischen, petrochemischen und feinchemischen Industrie. Durch das Verständnis der gängigen Reaktionstypen von homogenen Edelmetallkatalysatoren können Wissenschaftler effizientere und nachhaltigere chemische Prozesse entwickeln.
Stanford Advanced Materials (SAM) ist ein zuverlässiger Lieferant von Platinkatalysatoren, Palladiumkatalysatoren und anderen Edelmetallkatalysatoren. Schicken Sie uns eine Anfrage, wenn Sie interessiert sind.
Referenz:
[1] Shimbayashi, Takuya & Fujita, Ken-Ichi. (2020). Metall-katalysierte Hydrierungs- und Dehydrierungsreaktionen für effiziente Wasserstoffspeicherung. Tetrahedron. 76. 130946. 10.1016/j.tet.2020.130946.
[2] Azman, Nur & Ramli, Muhammad & Isa, Siti. (2019). A Review of hybridization of carbon nanotube into graphene for gas sensor application. IOP Conference Series: Materials Science and Engineering. 551. 012017. 10.1088/1757-899X/551/1/012017.
[3] Budiman, Anatta & Nam, Ji & Park, Jae & Mukti, Ryan & Chang, Tae & Bae, Jong Wook & Choi, Myoung. (2016). Review of Acetic Acid Synthesis from Various Feedstocks Through Different Catalytic Processes. Catalysis Surveys from Asia. 20. 10.1007/s10563-016-9215-9.

 Bars
Bars
 Perlen & Kugeln
Perlen & Kugeln
 Bolzen & Muttern
Bolzen & Muttern
 Tiegel
Tiegel
 Scheiben
Scheiben
 Fasern & Stoffe
Fasern & Stoffe
 Filme
Filme
 Flocke
Flocke
 Schaumstoffe
Schaumstoffe
 Folie
Folie
 Granulat
Granulat
 Honigwaben
Honigwaben
 Tinte
Tinte
 Laminat
Laminat
 Klumpen
Klumpen
 Maschen
Maschen
 Metallisierte Folie
Metallisierte Folie
 Platte
Platte
 Pulver
Pulver
 Stab
Stab
 Blätter
Blätter
 Einkristalle
Einkristalle
 Sputtering Target
Sputtering Target
 Rohre
Rohre
 Waschmaschine
Waschmaschine
 Drähte
Drähte
 Umrechner & Rechner
Umrechner & Rechner
 Chin Trento
Chin Trento



